Teori yang saya maksud adalah Teori Elektron. Teori inilah yang akan memberimu pengetahuan dasar mengenai partikel elektron, yang keberadaan sudah disadari oleh Sir Joseph John Thomson sejak puluhan tahun silam.
 |
| Sir Joseph John Thomson |
Perbedaan Zat, Molekul dan Atom
Pastinya kita sudah mengenal tiga macam wujud zat (padat, cair dan gas). Zat terbentuk dari susunan molekul-molekul, yaitu bagian paling kecil dari zat yang masih memiliki sifat-sifat seperti zat.
Molekul itu sendiri terbentuk dari susunan atom-atom, namun atom-atom itu sudah beda-sifat dengan molekul yang dibentuknya.
Struktur Dasar sebuah Atom
Gambarannya begini, atom itu memiliki bagian inti yang 'diselimuti' oleh berlapis-lapis kulit. di dalam inti terdapat partikel-partikel pembawa muatan positif (dinamai Proton), sedangkan pada setiap lapisan kulit terdapat partikel-partikel pembawa muatan nagatif (dinamai Elektron).
 |
| Struktur Dasar Atom |
Setiap lapisan kulit atom berisi partikel elektron dalam jumlah maksimal tertentu. Contohnya, kulit paling dalam berisi maksimal 2 elektron, dan kulit terluar bisa terisi maksimal 8 elektron. Elektron di kult terluar inilah yang menentukan kestabilan sebuah atom.
Elektron pada setiap lapisan kulit atom beredar mengelilingi inti atom sesuai dengan lintasannya masing-masing. Elektron-elektron bisa tetap terjaga pada lintasannya berkat adanya gaya tarik dari inti atom.
Hukum Coulomb
Elektron mendapatkan gaya tarik dari inti atom pada dasarnya gaya tarik itu berasal dari proton yang terkandung di dalam inti atom. Besarnya gaya itu dinyatakan dinyatakan oleh Hukum Coulomb yang berbunyi,
Besar gaya F antara dua titik muatan listrik (q1 dan q2) berbanding lurus dengan besar masing-masing muatan, dan berbanding terbaik dengan kuadrat jarak kedua titik muatan itu (r).
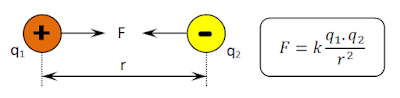 |
| Gaya Tarik antar Muatan Listrik |
- F, gaya antar muatan (Newton)
- q1, titik muatan pertama (Coulomb)
- q2, titik muatan kedua (Coulomb)
- r, jarak kedua titik muatan (meter)
- k, konstanta
Telah disebutkan di muka bahwa kestabilan sebuah atom ditentukan oleh elektron-elektron di kulit terluar atom yang bersangkutan. Syaratnya adalah di kult terluar itu harus terisi 8 elektron.
Ikatan antar Atom
Bagaimana jika syarat kestabilan itu belum terpenuhi? Salah satu cara yang ditempuh adalah dengan membentuk ikatan antara atom-atom terdekat guna melakukan "pemakaian bersama" elektron-elektron yang ada. Contoh kasus pada atom silikon yang memiliki 4 atom di kulit terluarnya.
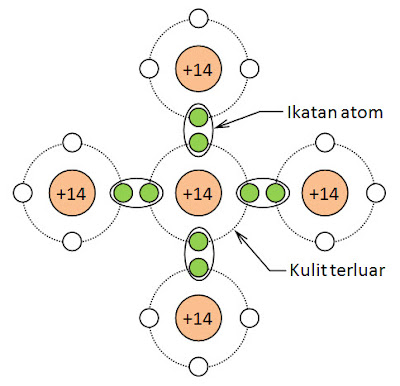 |
| Ikatan pada Atom Silikon |
Setiap atom dalam bahan silikon melakukan ikatan dengan 4 atom sesama terdekat guna mendapatkan "tambahan" 4 elektron yang dibutuhkannya untuk mencapai kondisi stabil.
Ikatan Logam
Atom pada bahan logam juga mengalami ikatan (disebut ikatan logam) seperti pada bahan silikon. Ikatan logam menentukan sifat fisik dan sifat listrik dari logam yang bersangkutan seperti permukaannya mengkilap, bisa dibengkokkan, dan penghantar listrik (konduktor) yang baik.
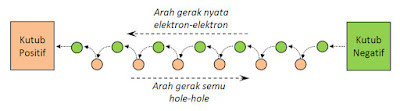
Elektron pada ikatan logam mudah lepas dari atomnya dan berubah menjadi elektron bebas (free electron). Pada tempat yang ditinggalkannya itu terbentuk hole. Hole pada sebuah atom merupakan pendukung muatan positif untuk atom tersebut.
Sesuai namanya, elektron bebas mudah sekali mengalami perpindahan dari satu hole ke hole lainnya. Jika perpindahan itu terjadi secara estafet, terbentuklah aliran muatan negatif yang dikenal sebagai arus elektron.

0 Tanggapan untuk "Jangan Pelajari Apapun, Sebelum Kamu Sentuh Teori Ini!"
Posting Komentar
Silahkan ajukan pertanyaan, kritik, dan saran tentang materi ini melalui form komentar di bawah. Thanks sebelumnya atas tanggapan yang kamu berikan.